Synthagen Laboratories
Tecnologia NL-PEPTIDI CONSEGNA™ come metodo innovativo per la creazione di peptidi di nuova generazione Confronto dell'azione e della durata dei peptidi tradizionali rispetto al metodo innovativo di sintesi e somministrazione orale dei peptidi.
Riassunto: Nella pratica, solo pochi peptidi tradizionali trovano applicazione a causa della loro instabilità biologica e rapida degradazione. La soluzione a questo problema è la modificazione peptidica, che consente di ottenere forme peptidiche stabili ed efficaci. I peptidi di nuova generazione, ottenuti tramite sintesi con la tecnologia NL-PEPTIDES, sono racchiusi in una doppia capsula, creata nel sistema NL-PEPTIDES DELIVERY ™, che permette di massimizzare l'efficacia e la stabilità del peptide.
Elenco abbreviazioni: •AFP- Peptidi Farmaceuticamente Attivi • NL-PEPTIDES- Peptidi di nuova generazione •NL-PEPTIDES DELIVERY- Tecnologia di somministrazione orale
Parole chiave: •peptide •legame peptidico• analogo• modificazione• salificazione• amidazione• acetilazione •sintesi• tecnologia• salificazione• arginina
Introduzione
La tecnologia NL-PEPTIDES DELIVERY ™, come metodo innovativo, permette di ottenere un effetto terapeutico superiore a quello dei peptidi tradizionali. L'efficacia di NL-PEPTIDES DELIVERY ™ è stata confermata sulla base delle risposte relative alla produzione di peptidi che arrivano intatti all'intestino, dove vengono poi completamente assorbiti. La tecnologia innovativa NL-PEPTIDES DELIVERY ™ è protetta da brevetto come nuova forma di analoghi peptidici per lo sviluppo e la commercializzazione di peptidi orali con un sistema speciale di somministrazione.
COSA SONO I PEPTIDI TRADIZIONALI
Dal punto di vista chimico tipico, i peptidi si presentano in forma lineare, possedendo solo due estremità specifiche. Una di queste è chiamata estremità amminica, dove l'amminoacido presenta un gruppo libero α-amminica. La seconda è chiamata estremità carbossilica o estremità C, dove l'amminoacido presenta un gruppo libero α-carbossilica. I peptidi sono composti chimici costruiti in modo simile alle proteine, a partire da amminoacidi. Sono oggetto di ampio interesse, svolgendo importanti funzioni biologiche. Molti ormoni e neurotrasmettitori sono proprio peptidi. Nel caso dei peptidi endogeni, essi agiscono con effetto antimicrobico, fungendo da sistema di difesa dell'organismo. I peptidi naturalmente presenti sono considerati composti attraenti di rilevanza terapeutica grazie all'elevato grado di attività, bassa tossicità e assenza di interazioni con farmaci. Nella pratica medica, solo pochi peptidi trovano applicazione a causa della loro instabilità biologica e rapida degradazione. La soluzione a questo problema di stabilità del peptide è la loro sintesi, che consente di ottenere forme peptidiche stabili. Lo stesso vale per la sintesi di peptidi da fonti naturali, utilizzati tra l'altro per la produzione di vaccini.
LEGAME PEPTIDICO
Carbone, a seguito della reazione del gruppo αdel gruppo carbossilico si lega all'azoto del gruppo αdel gruppo amminico tramite un legame singolo, il legame peptidico. Si presume che questo legame esista in due strutture che rimangono in un equilibrio reciproco definito. Il legame C-N passa a C=N e viceversa. La rotazione attorno all'asse C=N non è possibile, per cui il legame peptidico è abbastanza rigido da possedere le caratteristiche di un legame doppio. Gli amminoacidi che partecipano alla formazione del legame peptidico perdono frammenti di molecole. Si tratta di molecole -OH dal gruppo carbossilico e -H dal gruppo amminico. Per questo motivo, gli amminoacidi presenti nei peptidi e nelle proteine sono chiamati residui amminoacidici. I legami peptidici formati sono stabili e la loro rottura può avvenire solo sotto l'azione di basi e acidi forti a temperature elevate.
SINTESI DEI PEPTIDI
A seconda del peptide che vogliamo ottenere, abbiamo bisogno del metodo appropriato per la sua sintesi. In una breve spiegazione cercheremo di presentare la sintesi dei peptidi in riferimento a in base alla sua dimensione. Per ottenere il dipeptide si deve utilizzare un reagente che porta a dell'attivazione del gruppo carbossilico dell'amminoacido acilante o effettuare una modifica amminoacido acilante in anidride. Un processo più laborioso e complesso è la sintesi nel caso di peptidi più grandi, che otteniamo dal dipeptide, dove avviene rimozione della protezione del gruppo amminico dell'amminoacido N-terminale e la sua acilazione con il successivo protetto N-terminalmente. Questo processo è particolarmente dispendioso in termini di tempo, poiché le suddette operazioni si ripetono fino a ottenere il peptide della lunghezza pianificata della sequenza. Nel caso di peptidi di grandi dimensioni, il metodo più efficace e il metodo più semplice è il metodo di Merrifield. Questo metodo viene eseguito nella fase costante. L'amminoacido C-terminale si attacca al polimero, dove successivamente si lega del successivo amminoacido, fino al momento in cui si raggiunge la lunghezza desiderata łcatena.
ANALOGHI DI PEPTIDI
In risposta alla natura instabile dei peptidi tradizionali, vengono progettati e prodotti i loro analoghi. Gli analoghi peptidici sono definiti come appropriati composti chimici, grazie a in cui un atomo è sostituito da un altro rispetto al composto di partenza. La generale la struttura del peptide rimane invariata. Tra gli analoghi peptidici vi sono analoghi con struttura dell'elica e analoghi βpiegature e βpagine. Nel primo di essi eliche sono uno degli elementi strutturali chiave dei peptidi bioattivi. La stabilizzazione di brevi frammenti di oligomeri in conformazione elicoidale aumenta l'attività. Negli analoghi βpiegature e βalle pagine avviene l'inserimento di residui D-amminoacidici o β,γ,δ-amminoacidici. Gli analoghi peptidici ci permettono di ottenere nuovi composti peptidici, più stabili, che trovano applicazione in un più ampio spettro sintomatico e consentono soluzioni innovative ai problemi legati all'azione delle forme preesistenti.
ANALOGHI PEPTIDICI ATTRAVERSO MODIFICHE
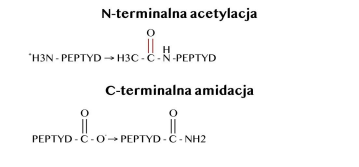
I peptidi tradizionali, nonostante i numerosi e indiscutibili vantaggi, presentano anche molte limitazioni legate al loro utilizzo. La ricerca di nuovi analoghi peptidici massimamente stabili, con un ampio spettro d'azione, è la conseguenza dell'esistenza di peptidi tradizionali poco stabili. Analoghi dei peptidi tradizionali contenenti la sequenza la chiave del peptide è arricchita con modifiche effettuate all'interno della catena peptidico o della catena laterale dei residui amminoacidici presenti nella sequenza. L'introduzione di amidazione e acetilazione contribuisce a migliorare la stabilità metabolica e selettività. Tra gli esempi noti di modifiche, a seconda del profilo d'azione che si vuole caratterizzare un peptide, tra cui acetilazione dell'N-terminale, ciclizzazione, marcatura con fluorofori, amidazione del C-terminale del peptide o D-amminoacidi.
PROCESSO DI SALIFICAZIONE DEI PEPTIDI
Il processo di salificazione consiste nella modifica delle cariche proteiche. Le cariche della proteina vengono neutralizzate da anioni e cationi del sale. Le molecole proteiche non si attraggono e non formano aggregati, e la proteina stessa precipita a causa della perdita del mantello acquoso. Il processo di salificazione è reversibile. Nel processo inverso, il sale viene rimosso tramite dialisi o la sua concentrazione viene ridotta aggiungendo acqua. La salificazione, mediante l'aggiunta di molecole di arginina, porta alla formazione di una forma stabile del peptide ed è un metodo innovativo per garantire la stabilità peptidica e quindi ampliare l'azione biologica dei peptidi.

ACETILAZIONE E AMMIDAZIONE DEL PEPTIDE
L'acetilazione dell'N-terminale del peptide consiste nell'aggiunta di radicali acetilici ai substrati, che sono composti con gruppi NH2, OH o SH, con l'ausilio dell'enzima N-acetiltransferasi. La fonte del radicale acetilico è l'acetil-CoA. La funzione principale delle N-acetiltransferasi è facilitare il legame del gruppo acetile con il gruppo amminico degli amminoacidi aromatici e delle idrazine (reazione di N-acetilazione), ovvero la detossificazione di composti esogeni potenzialmente tossici. Quando si verifica la rottura dei legami peptidici e di conseguenza la frammentazione della catena polipeptidica, si formano gruppi carbonilici. L'ossidazione della molecola proteica da parte del radicale ossidrile inizia con la rimozione di un atomo di idrogeno dal carbonio α amminoacido. Il radicale alchilico formato reagisce con l'ossigeno formando un radicale alchilperossido che si trasforma in alchilidroperossido. Il radicale alcoxilico che si forma può trasformarsi in un idrossilato sul carbonio α del residuo amminoacidico o può portare alla frammentazione della catena polipeptidica. La presenza del radicale alcoxilico favorisce la frammentazione della catena polipeptidica. La scissione del legame peptidico può avvenire tramite αamidazione o diamidazione. Durante la formazione αdi frammentazione amidica N-terminale, il peptide ha al C-terminale un gruppo ammidico, mentre l'altro peptide contiene al N-terminale un derivato N-α-ketoacilica. La frammentazione tramite diamidazione è caratterizzata dalla formazione di un peptide N-terminale contenente una struttura diamidica e di un peptide derivato dal C-terminale della molecola proteica contenente all'N-terminale una struttura isocianato.
COS'È NL-PEPTIDES™
In risposta alle problematiche relative alla produzione di peptidi che raggiungono intatti l'intestino, abbiamo creato un gruppo di nuovi peptidi, chiamati NL-peptidi, noti anche come peptidi di nuova generazione, contrassegnati con l'abbreviazione AFP. Le caratteristiche dei peptidi attivi farmacologicamente riflettono il loro vantaggio rispetto ai peptidi tradizionali. Si distinguono principalmente per una maggiore durata e resistenza alle variazioni di pH e temperatura, sia durante la conservazione del prodotto sia nell'ambiente del sistema digestivo, dove al momento dell'assunzione della capsula e del suo trasporto all'intestino tenue, il peptide non subirà degradazione. Il gruppo di NL-peptidi si caratterizza per la capacità di imitare le proteine naturali e per l'elevata stabilità metabolica, grazie alla quale i NL-peptidi, agendo come proteine naturali, vengono assorbiti intatti dall'intestino e non subiscono degradazione durante l'assorbimento.
CREAZIONE DEI NL-PEPTIDES ™ TRAMITE SINTESI
La rappresentazione chimica dei NL-peptidi, ottenuti tramite modifiche attraverso la sintesi, sarà discussa di seguito, La tecnologia, che agisce sul principio della salificazione del peptide con arginina, è stata arricchita mediante la sintesi tramite N-acetilazione dell'estremità amminica del peptide con contemporanea amidazione dell'estremità carbossilica del legame. L'insieme dei processi modificativi eseguiti si traduce in un aumento di 10 volte della stabilità dei NL-PEPTIDI e nella menzionata capacità di imitare le proteine naturali.
TECNOLOGIA NL-PEPTIDES DELIVERY ™
Affrontando il compito di creare una tecnologia moderna per la somministrazione orale di peptidi, è stato fondamentale risolvere i problemi relativi, innanzitutto, alla creazione di una tecnologia semplice basata sulla versatilità, in riferimento a una vasta gamma di prodotti, nonché alla produzione simultanea di più prodotti efficaci in un unico momento, grazie a un metodo che consente di sviluppare un sistema che permette tale schema operativo. I problemi finora legati all'assorbimento sono stati risolti mediante l'uso delle sole modifiche peptidiche menzionate. Nel nostro caso, oltre alla modifica del peptide, ci siamo concentrati su una soluzione indubbiamente importante al problema legato al trasporto del peptide, dal momento della somministrazione orale, attraverso il passaggio all'intestino tenue fino al momento dell'assorbimento della sostanza. La soluzione ai problemi tecnologici menzionati è la creazione di una nuova tecnologia semplice ed efficace per la somministrazione del peptide, che definiamo come NL-PEPTIDES-DELIVERY ™
PROFILO D'AZIONE DELLA TECNOLOGIA NL-PEPTIDES DELIVERY ™
Il profilo d'azione, basato sulla tecnologia NL-PEPTIDES DELIVERY, consente principalmente il raggiungimento del peptide nell'intestino tenue, attraverso un rivestimento appositamente creato a questo scopo che avvolge il NL-peptide. Oltre al semplice raggiungimento del peptide nell'intestino tenue, è importante che l'intero ambiente locale presente nell'intestino sia favorevole all'assorbimento del peptide somministrato in quel punto. Il problema era significativo a causa degli enzimi-peptidasi presenti nell'intestino, che degradano i peptidi. I principali enzimi che degradano i peptidi sono gli enzimi proteolitici, chiamati proteasi, che impediscono il proseguimento del peptide degradandolo nell'intestino tenue. Il fattore che rappresentava un problema, e che abbiamo risolto, è la scarsa assorbimento del peptide stesso attraverso la parete dell'intestino tenue.
VANTAGGI DELLA TECNOLOGIA NL-PEPTIDES DELIVERY ™
Concentrandosi sul profilo d'azione specifico della tecnologia NL-PEPTIDES DELIVERY ™, esso consiste nello sviluppo di una nuova capsula doppia con rivestimenti protettivi, che risolve il problema sia del raggiungimento del peptide nell'intestino tenue sia del suo passaggio attraverso la parete intestinale e della degradazione del peptide in questo punto. Il rivestimento protettivo, che costituisce la superficie più esterna della capsula, protegge il composto dai cambiamenti di pH e dall'acido gastrico, permettendo al peptide di raggiungere l'intestino. Grazie all'uso dell'inibitore della proteasi nella composizione della capsula, il peptide soggetto a degradazione non si decompone, abbassando contemporaneamente il pH locale dell'intestino e preparando l'ambiente per l'assorbimento del peptide. Il potenziatore dell'assorbimento è stato utilizzato per migliorare l'assorbimento del peptide nell'intestino tenue. Il NL-peptide è stato rivestito da uno strato che lo separa dall'inibitore della proteasi. L'inibitore stesso è un acido che, se a contatto con il peptide, potrebbe degradarlo. Separandolo dall'acido tramite la capsula nella capsula, abbiamo ottenuto una composizione farmaceutica stabile e non degradabile durante la conservazione.
FUNZIONAMENTO DELLA TECNOLOGIA NL-PEPTIDES DELIVERY ™ NEL SISTEMA DIGERENTE
Peptidi di nuova generazione, creati tramite sintesi con la tecnologia NL-PEPTIDES. Racchiusi in una capsula doppia creata nel sistema NL-PEPTIDES DELIVERY ™, che durante la somministrazione orale segue un percorso specifico nel sistema digestivo. La capsula ingerita arriva intatta all'intestino tenue, dove avviene il rilascio dell'inibitore della proteasi, creando così un ambiente adatto all'assorbimento abbassando il pH dell'intestino a 5,5. Nella fase successiva avviene il rilascio del principio attivo e del potenziatore dell'assorbimento, permettendo al peptide di essere efficacemente assorbito dall'organismo.
RISULTATI DELL'UTILIZZO DELLA TECNOLOGIA NL-PEPTIDES DELIVERY ™
Il confronto dei risultati della somministrazione orale, sotto forma di capsula doppia, rispetto alla somministrazione del peptide tramite spray nasale permette di determinare la superiorità e l'efficacia di una delle due modalità di somministrazione. La concentrazione del peptide al momento della somministrazione orale, nella nostra capsula, è molto più alta rispetto alla concentrazione del peptide nella somministrazione nasale. Durante lo studio sono state utilizzate le stesse dosi di peptide sia nella capsula che nello spray nasale. I risultati di questi studi evidenziano il vantaggio della nostra tecnologia rispetto alla somministrazione nasale.
RISULTATO DEL LAVORO DI SYNTHAGEN LABORATORIES
Il compito che ci siamo posti riguardava la creazione di una nuova tecnologia che consente di aumentare l'efficacia dell'azione dei peptidi. La tecnologia di somministrazione orale dei peptidi NL-PEPTIDES-DELIVERY si basa su una terapia peptidica innovativa insieme a un metodo di somministrazione orale all'avanguardia, creato da noi. La presentazione multicanale della nostra tecnologia permette di comprendere in dettaglio ciascuna delle sue fasi.
In modo illustrativo, gli effetti del nostro lavoro possono essere visti nella presentazione





Peptidi con proprietà antimicrobiche e i loro analoghi ottenuti mediante modifiche.
Ruolo del peptide NL GHK-Cu nei processi di ricostruzione e rigenerazione della pelle e dei capelli