Les acides aminés de différentes longueurs de chaîne et de séquences variées peuvent former des dimères et des polymères. Selon le nombre de résidus d'acides aminés situés sur la chaîne polymérique, les polymères se divisent en peptides et protéines. Les peptides contiennent environ 50 acides aminés dans leur structure, tandis que les protéines contiennent dans une ou plusieurs chaînes un nombre de résidus d'acides aminés supérieur à celui des peptides. Les acides aminés, les protéines et les peptides jouent tous un rôle essentiel dans le bon fonctionnement de l'organisme. Grâce aux thérapies peptidiques modernes, il est possible de favoriser la régénération de l'organisme.
Mots-clés : peptide · acide aminé · protéine · hélice α · structure β · chaîne non polaire · alanine · valine · leucine · isoleucine · phénylalanine · tryptophane · méthionine · proline · glycine · sérine · thréonine · tyrosine · cystéine · asparagine · glutamine · acide aspartique · acide glutamique · configuration · conformation · dipeptide · oligopeptide · liaison peptidique · hormone de croissance
Liste des abréviations : ACTH - adrénocorticotrophine ; CRH - corticolibérine ; POMC - pro-opiomélanocortine ; MMC - complexe moteur migrant ; GRPP - polypeptide pancréatique dépendant de la glycentine ; HGH - hormone de croissance. Le rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme, présenté ci-dessous, permet de comprendre leur action ainsi que les possibilités qu'ils offrent.
Caractéristique des acides aminés
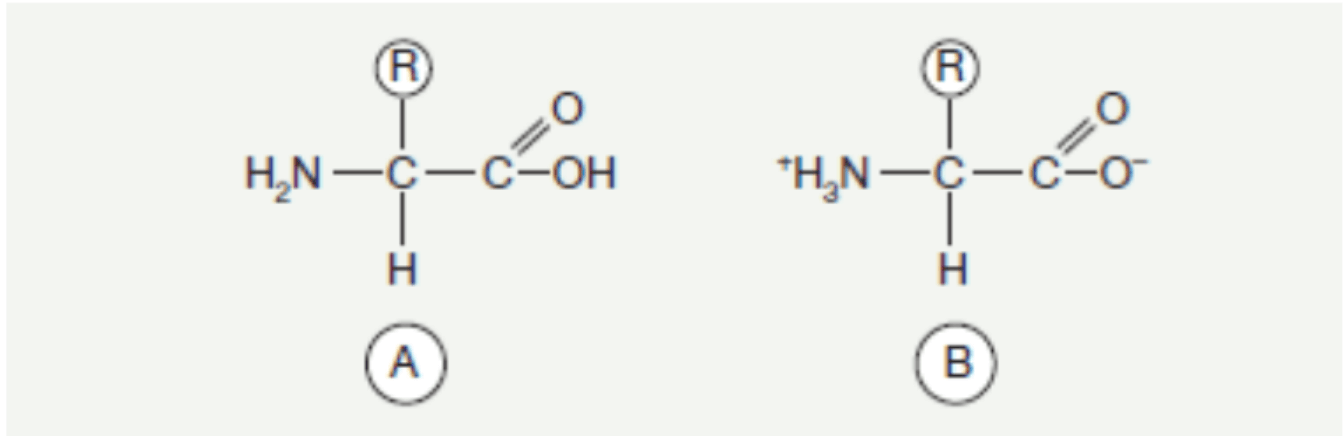
Les acides aminés, parmi les composants les mieux connus des organismes vivants, se présentent comme des dérivés d'acides organiques, où au moins un atome d'hydrogène est remplacé par un groupe amine. Ils sont des composants courants, présents à la fois sous forme libre et liée - dans le cas des peptides ou des protéines. Chacun des acides aminés présents dans les protéines, à l'exception de la proline et de l'hydroxyproline, possède un groupe amine situé sur le carbone α et une chaîne latérale R, qui peut avoir une structure variable et est liée au même atome de carbone.
Formule générale d'un acide aminé.
A. Sous forme libre
B. Sous forme de zwitterion. Environ 300 acides aminés sont connus dans l'environnement, mais 22 sont couramment présents, dont 2 supplémentaires ont été découverts relativement récemment et ne se trouvent que dans certaines protéines. La présence et la localisation dans la structure protéique des acides aminés déjà connus sont déterminées par des propriétés génétiques ; dans certains cas, cela résulte d'une modification post-traductionnelle des résidus d'acides aminés qui ont été préalablement incorporés dans la chaîne protéique. Les autres acides aminés peuvent exister sous forme libre ou dans des composés non protéiques. Le rôle d'un acide aminé dans une protéine est déterminé par la structure de sa chaîne latérale, ce qui conduit à une classification des acides aminés en plusieurs groupes, selon la nature des chaînes latérales qu'ils possèdent.
Acides aminés à chaînes non polaires
Le groupe des acides aminés à chaînes non polaires comprend successivement : alanine, valine, leucine, isoleucine, phénylalanine, tryptophane, méthionine, proline et glycine. Pour les deux derniers acides aminés mentionnés, il existe une certaine relation. La proline, en tant qu'exemple atypique, ne possède pas de groupe α-aminé mais un groupe imino, qui est intégré dans la structure de l'anneau pyrrolidine. Rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme. La glycine, quant à elle, ne possède pas de chaîne latérale, remplacée par un atome d'hydrogène. Chacun des acides aminés mentionnés possède une chaîne latérale non polaire, qui n'a pas la capacité de capter ou de perdre des protons et ne participe pas à la formation de liaisons hydrogène ou ioniques. La chaîne latérale est le plus souvent considérée comme lipophile, c’est-à-dire hydrophobe – ne liant pas l'eau. Ces chaînes évitent l'environnement aqueux en s'agrégeant et sont orientées vers l'intérieur de la molécule protéique. Lorsqu'elles se trouvent dans un milieu aqueux, leur comportement est comparable à celui de gouttes d'huile, qui se regroupent en gouttes plus grosses, réduisant ainsi le contact avec l'eau.
Acides aminés avec des chaînes latérales polaires sans charge
Le groupe des acides aminés à chaînes latérales polaires non chargées comprend : la sérine, la thréonine, la tyrosine, la cystéine, l'asparagine et la glutamine. Ces acides aminés ont une charge nulle en milieu à pH neutre, mais dans le cas de la cystéine et de la tyrosine, ils peuvent perdre un proton en milieu basique. La sérine, la thréonine et la tyrosine peuvent former des liaisons hydrogène grâce à leur groupe hydroxyle polaire. De même, les chaînes latérales de l'asparagine et de la glutamine peuvent former des liaisons hydrogène en raison de leurs groupes carbonyle et amide. Le groupe amide de l'asparagine ainsi que les groupes hydroxyle de la sérine et de la thréonine peuvent être des sites de liaison pour des composants glucidiques. Rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme.
Acides aminés à chaînes acides
Le groupe des acides aminés à chaînes acides comprend l'acide aspartique et l'acide glutamique. Les chaînes latérales de ces acides aminés présentent des groupes carboxyle. En milieu à pH neutre, ils subissent une dissociation complète, devenant porteurs d'une charge négative. Les formes complètement ionisées de l'acide aspartique et de l'acide glutamique sont appelées aspartate et glutamate. Ces noms transformés, après ionisation, indiquent qu'à un pH physiologique, ils sont des anions. Rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme
Acides aminés à chaînes basiques
Acides aminés à chaînes basiques. Le groupe des acides aminés à chaînes basiques comprend : la lysine, l'arginine et l'histidine. Les chaînes latérales de ces acides aminés contiennent des groupes capables de lier des protons. Ces groupes incluent le groupe ε-amine de la lysine, le groupe guanidinium de l'arginine et l'anneau imidazole de l'histidine. Au pH physiologique, les groupes R de la lysine et de l'arginine sont complètement ionisés, ce qui leur confère une charge positive. L'acide aminé libre qu'est l'histidine a un caractère légèrement basique et se trouve sous forme neutre au pH physiologique. Cependant, il peut arriver que l'histidine dans une protéine possède un groupe R chargé positivement ou neutre, selon l'environnement créé par la protéine. Cela joue un rôle important dans le fonctionnement de la protéine qu'est l'hémoglobine.
Protéines
Caractéristiques des protéines
Les protéines, en tant que polymères condensés d'acides aminés, qui sont abondants dans l'organisme humain, constituent un composant structurel fondamental pour son bon fonctionnement. Composées uniquement de résidus d'acides aminés, elles sont appelées protéines simples ou protides. Les protéines complexes, ou protéides, contiennent en plus un groupe prosthétique qui n'est pas un composant protéique. En tant que produits macromoléculaires, elles résultent de l'interaction du groupe α-carboxyle d'un acide aminé avec le groupe α-amine d'un autre acide aminé, formant une liaison peptidique. On appelle polypeptides les protéines dont la masse moléculaire est supérieure à 10 000 daltons (Da). Toutes les protéines ayant une masse moléculaire inférieure sont appelées oligopeptides. Chaque protéine possède une chaîne protéique composée de 100 à 1000 résidus d'acides aminés.
Structure primaire
La structure primaire de la chaîne polypeptidique d'une protéine donnée détermine l'ordre (séquence) de liaison des résidus d'acides aminés dans la chaîne polypeptidique. Les acides aminés individuels sont liés de manière covalente par des liaisons peptidiques. Dans les protéines, seules certaines séquences d'acides aminés existent en raison du grand nombre de combinaisons possibles. La disposition des résidus d'acides aminés le long de la chaîne polypeptidique n'est pas strictement et clairement définie. À travers l'exemple de la molécule de protéine qu'est l'hémoglobine, on peut souligner l'importance de la structure primaire. Dans ce cas, le remplacement d'un acide aminé par un autre entraîne la formation d'une hémoglobine pathologique. Pour mieux comprendre l'origine de cette formation, par exemple, en position six, l'acide glutamique est remplacé par un autre acide aminé (valine ou lysine), ce qui conduit à des conséquences biologiques négatives. Les globules rouges subissent une modification biologique, entraînant un changement de leur forme en une forme atypique. Les globules deviennent sensibles à l'hémolyse, ce qui provoque simultanément une diminution du nombre d'érythrocytes dans le sang. Les produits de dégradation des érythrocytes sont captés par le foie et la rate, et la concentration du pigment biliaire, la bilirubine, augmente suite à la dégradation de l'hème dans l'hémoglobine. Ces processus entraînent le développement d'une maladie appelée anémie hémolytique.
Structure secondaire
En parlant de la structure secondaire, les notions fondamentales sont celles de configuration et de conformation. Alors que la configuration se réfère aux relations géométriques entre des ensembles spécifiques d'atomes, la conformation concerne la structure spatiale de la protéine. Dans le cas de la configuration, il y a un changement mutuel de la construction des liaisons déjà formées, par exemple, la transformation de la D-alanine en L-arginine. Une telle conversion peut être obtenue en rompant les liaisons covalentes existantes et en les reformant. En revanche, la conformation ne conduit pas à la rupture des liaisons covalentes, mais à la rupture et à la reformulation des forces non covalentes, telles que les ponts hydrogène ou les interactions hydrophobes. Seules certaines conformations formées ont une importance biologique. La forme la plus courante de la structure secondaire des protéines est l'hélice α en forme de spirale. Un tour complet de l'hélice α correspond à 3,6 résidus d'acides aminés. Le rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme. La forme spirale spécifique et différente des autres permet la formation de liaisons hydrogène, à l'intérieur de la chaîne et entre les tours, avec une force maximale, en raison des interactions électrostatiques possibles. La structure de l'hélice α, incluant la liaison peptidique de la chaîne protéique, permet sa participation à la formation de liaisons hydrogène, à l'exception des liaisons impliquant les groupes imine de la proline. Les polypeptides obtenus par synthèse à partir d'acides aminés L ou D forment spontanément une structure d'hélice α. Dans le cas des polypeptides issus de racémats d'acides aminés ainsi que des polymères de certains acides aminés, par exemple la proline ou l'hydroxyproline, ils ne possèdent pas la capacité de former spontanément cette structure. Par exemple, l'α-kératine, qui est une protéine présente notamment dans les cheveux et est presque entièrement constituée d'une structure d'hélice α, tandis que le collagène ou l'élastine, qui contiennent la proline et l'hydroxyproline mentionnées, ne possèdent aucune capacité à former cette structure.
Structure tertiaire
La structure tertiaire permet de conserver la structure secondaire, tout en pliant tridimensionnellement la molécule protéique. Le rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme 7. L'agencement spatial de la molécule protéique est principalement déterminé par la structure primaire, et indirectement par la structure secondaire. La structure tertiaire est stabilisée par des interactions entre les chaînes latérales des résidus d'acides aminés, incluant des liaisons covalentes, notamment des ponts disulfures, ainsi que par des liaisons non covalentes de faible énergie, comme les liaisons hydrogène. Dans les solutions aqueuses, la structure des protéines globulaires est compacte. Les chaînes latérales hydrophobes des résidus d'acides aminés sont cachées à l'intérieur de la molécule, tandis que les groupes hydrophiles se trouvent à la surface. Les groupes polaires, y compris ceux cachés à l'intérieur de la molécule, ainsi que les éléments constituant les liaisons peptidiques, permettent la formation de liaisons hydrogène et d'interactions électrostatiques. La structure tertiaire ne se forme que lorsqu'il existe des liaisons permettant de relier des résidus d'acides aminés éloignés linéairement.
Structure quaternaire
La dernière des structures présentées n'apparaît que dans certaines protéines et détermine l'agencement spatial ainsi que la composition des sous-unités par rapport à une molécule protéique unique. Dans ce cas, les protéines ont une masse moléculaire élevée et sont composées de deux monomères ou plus, c'est-à-dire de chaînes peptidiques. Généralement, dans le cas de la structure quaternaire, les éléments protéiques participant à sa formation sont reliés par des liaisons hydrogène de faible énergie. Dans certains cas, la structure est stabilisée par des ponts disulfures entre les résidus de cystéine. Pour le collagène et l'élastine, les liaisons covalentes entre les sous-unités sont exceptionnellement stables. Les propriétés biologiques de la structure quaternaire peuvent être modifiées par des petites molécules appelées effecteurs allostériques. Dans le cas de l'hémoglobine et des protéines enzymatiques, en particulier la déshydrogénase lactique, la structure quaternaire est très bien connue. Le rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme.
Peptides
Caractéristique des peptides
Les peptides sont des composés chimiques construits de manière similaire aux protéines, à partir d'acides aminés. Ils suscitent un large intérêt en remplissant des fonctions biologiques importantes. De nombreuses hormones ainsi que des neurotransmetteurs sont précisément des peptides. Dans le cas des peptides endogènes, ils agissent comme agents antimicrobiens, servant de système de défense de l'organisme. Les peptides naturellement présents ainsi que leurs analogues synthétiques sont considérés comme des composés attrayants d'un point de vue thérapeutique en raison de leur haute activité, faible toxicité et absence d'interactions médicamenteuses. En pratique médicale, seuls quelques peptides sont utilisés en raison de leur instabilité biologique et de leur dégradation rapide, mais la synthèse des peptides permet d'obtenir des formes stables. C'est également le cas, par exemple, de la synthèse de peptides à partir de sources naturelles, qui sont utilisées notamment pour la production de vaccins. Le produit résultant de la réaction de deux acides aminés est appelé dipeptide, en conservant un groupe amine libre sur l'un des acides aminés et un groupe carboxyle libre sur l'autre. Les peptides composés de quelques à une dizaine d'acides aminés sont appelés oligopeptides, tandis que les peptides plus longs, contenant plusieurs dizaines de résidus d'acides aminés, sont des polypeptides. La nomenclature des peptides commence par le nom du résidu d'acide aminé N-terminal, suivi des noms des résidus d'acides aminés successifs, et se termine par le nom de l'acide aminé C-terminal. L'ordre des acides aminés est noté à l'aide de symboles à trois lettres ou à une lettre. Les peptides existent sous une forme linéaire, possédant seulement deux extrémités spécifiques. L'une est appelée extrémité amine, où se trouve un acide aminé avec un groupe α-amine libre. L'autre est appelée extrémité carboxyle ou extrémité C, où se trouve un acide aminé avec un groupe α-carboxyle libre.
Liaison peptidique
Le carbone issu de la réaction du groupe α-carboxyle se lie à l'azote du groupe α-amine par une liaison simple, la liaison peptidique. On suppose que cette liaison existe sous deux structures qui restent en équilibre mutuel défini. La liaison C-N passe en C=N et inversement. La rotation autour de l'axe C=N n'est pas possible, ce qui rend la liaison peptidique suffisamment rigide pour posséder les caractéristiques d'une liaison double. Rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme 9 Dans le cas de la liaison peptidique impliquant le groupe imine de la proline ou de l'hydroxyproline avec le groupe carboxyle d'un autre acide aminé, une structure différente et distincte se forme. L'azote est alors intégré dans la structure du cycle pyrrolidine, il n'y a pas de substituant hydrogène, ce qui empêche la rotation autour des liaisons formées en présence d'azote. Les acides aminés participant à la formation de la liaison peptidique perdent des fragments de molécules. Il s'agit de molécules -OH du groupe carboxyle et -H du groupe amine. C'est pourquoi les acides aminés présents dans les peptides et les protéines sont appelés résidus d'acides aminés. Les liaisons peptidiques formées sont stables et leur rupture ne peut se produire qu'en présence de bases et d'acides forts, simultanément à haute température.
Peptides biologiquement actifs
Les hormones peptidiques ainsi que les hormones protéiques sont couramment présentes dans notre environnement. Elles étaient auparavant majoritairement connues comme des formes peu stables. Grâce à la synthèse, il est désormais possible de choisir avec plus d'assurance une thérapie peptidique qui sera durable et efficace selon les besoins de l'organisme. C'est pourquoi il est intéressant de manipuler habilement et en toute sécurité la stimulation hormonale. En tenant compte de certains peptides biologiquement actifs, on peut citer par exemple le glutathion, qui, étant un tripeptide à structure spécifique, est composé de glutamate, cystéine et glycine. Le glutamate se trouve en position d'acide aminé N-terminal. La liaison entre le glutamate et la cystéine est cependant atypique pour les peptides et protéines, car ce n'est pas le groupe α-carboxyle du glutamate qui est impliqué, mais le groupe γ-carboxyle. Le glutathion existe donc sous forme réduite et oxydée, en tant que γ-glutamylcystéinylglycine. Sous forme réduite, il possède un groupe sulfhydryle libre, tandis que sous forme oxydée, une paire d'atomes d'hydrogène est détachée des groupes –SH. Les atomes de soufre restent alors dépourvus d'hydrogène, ce qui conduit à la formation d'un pont disulfure. La capacité du glutathion à passer de l'état oxydé à réduit est importante dans les processus d'oxydoréduction. Un autre exemple est l'ocytocine et la vasopressine, qui sont des nanopeptides produits par les neurones de l'hypothalamus et libérés par la posthypophyse, ne différant que par deux acides aminés. La cystéine se trouve en deux positions, ce qui conduit à la formation d'un pont disulfure. L'ocytocine agit comme une hormone stimulant les contractions utérines. La vasopressine, quant à elle, favorise la réabsorption d'eau dans les tubules rénaux. Elle joue également un rôle important dans la régulation de la sécrétion de l'hormone adrénocorticotrope (ACTH) en situation de stress. Le rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme.
Hormones peptidiques
Hormone adrénocorticotrope (ACTH)
L'hormone adrénocorticotrope, un peptide de 39 acides aminés, est produite par dégradation d'une molécule précurseur beaucoup plus grande, la pro-opiomélanocortine (POMC). La pro-opiomélanocortine est également la source d'autres peptides actifs. Deux peptides sont contenus dans la structure de l'ACTH. Il s'agit de l'hormone α-mélanotropique (α-MSH), identique dans sa structure aux 13 premiers acides aminés de l'ACTH, et du peptide de la partie intermédiaire de l'hypophyse, similaire à la corticotropine, fragment 18-39 de l'ACTH. La fonction principale de l'ACTH est de stimuler le cortex surrénalien afin qu'il puisse sécréter des hormones stéroïdes. L'hormone adrénocorticotrope régule l'activité des couches fasciculée et réticulée du cortex. Les 18 premiers acides aminés sont responsables de l'activité biologique de l'ACTH. La régulation de l'ACTH se fait par la corticolibérine (CRH), une hormone hypothalamique qui libère la corticotropine via le cortisol par rétrocontrôle négatif. Cela signifie qu'une carence en cortisol stimule la CRH et l'ACTH, tandis qu'un excès inhibe leur sécrétion. En libérant du cortisol, l'ACTH régule de nombreuses fonctions vitales, notamment la mobilisation de l'organisme en situation de stress, l'augmentation de la pression artérielle et les capacités anti-inflammatoires. Sécrété de manière pulsatile selon un rythme circadien, l'ACTH atteint sa concentration maximale le matin, moment où elle est la plus nécessaire, puis diminue au cours de la journée. Une augmentation de la sécrétion d'ACTH est observée dans des pathologies telles que l'insuffisance surrénalienne, la maladie de Cushing ou le syndrome de Nelson.
Insuline et peptide C
L'insuline et le peptide C sont sécrétés en continu par le pancréas chez l'être humain. Lors de la production d'insuline, au cours de sa biosynthèse, le peptide C est également produit. Les cellules pancréatiques produisent dans un premier temps la préproinsuline, qui subit une modification par clivage des acides aminés, conduisant à la formation de la proinsuline composée de deux chaînes, A et B, reliées par le peptide C. Ensuite, le peptide C est détaché de la proinsuline, ce qui donne la forme finale de l'insuline. Lorsqu'une augmentation de glucose apparaît dans l'organisme, le pancréas reçoit le signal de libérer des granules contenant des molécules d'insuline et de peptide C. Le rôle biologique des acides aminés, protéines et peptides est essentiel au bon fonctionnement et à la régénération de l'organisme. Le peptide C est maintenu dans le foie beaucoup plus longtemps que l'insuline, car il n'y est pas dégradé. Sa dégradation a lieu principalement dans les reins. Pour l'insuline comme pour le peptide C, une concentration trop élevée ou trop basse peut entraîner le développement d'un diabète de type I ou II ainsi que la maladie de Cushing. Pour le peptide C, les fluctuations de concentration peuvent également indiquer une insuffisance rénale chronique ou la présence de métastases ou de récidives locales de tumeur, d'où l'importance de maintenir des concentrations normales.
Motiline
La motiline est une hormone liée aux muscles lisses de l'estomac et des intestins, contrôlée par les fibres du nerf vague. Synthétisée dans les cellules endocrines, cette hormone peptidique composée de 22 acides aminés dans une séquence spécifique est produite par les cellules de l'intestin grêle. Produite par les cellules endocrines du système digestif M (Mo), elle participe à la régulation de la motricité du tube digestif. La motiline est une hormone importante impliquée dans la phase III du complexe moteur migrant (CMM), durant laquelle l'estomac et l'intestin grêle ont pour tâche de vider l'estomac des résidus alimentaires inutiles et des cellules épithéliales desquammées, en stimulant les mouvements péristaltiques. Cette hormone influence également la vidange de la vésicule biliaire pendant la période inter-digestive, au moment où la concentration de motiline est la plus élevée.
Glucagon
Le glucagon est l'une des hormones impliquées dans la régulation de la concentration de glucose ; ce peptide est sécrété par les cellules endocrines du pancréas. C'est un polypeptide composé de 29 acides aminés, issu d'un précurseur de 180 acides aminés. Les variations de la concentration de glucose permettent la sécrétion de glucagon. La production de cette hormone a lieu dans les îlots pancréatiques, où le proglucagon donne naissance au glucagon ainsi qu'au polypeptide pancréatique dépendant de la glicentine (GRPP). La principale fonction du glucagon est de maintenir une concentration normale de glucose dans le sérum lors de sa baisse entre les repas ou pendant l'effort physique. Ses réserves sont alors libérées par le foie pour assurer une protection adéquate de l'organisme. De plus, il peut participer à la régulation lors de la prise alimentaire, ce qui peut entraîner une sensation de satiété plus précoce. Le glucagon peut potentiellement inhiber la libération de ghréline ainsi que freiner la motilité intestinale. Rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme
Hormones protéiques
Hormone de croissance HGH L'hormone de croissance HGH est également appelée somatotropine. Elle est produite par les cellules acidophiles appartenant au lobe antérieur de l'hypophyse. Cette hormone conduit à une augmentation de la prolifération des cellules de divers tissus, ce qui se traduit par une augmentation de leur nombre et de leur taille. Le HGH est composé de 190 acides aminés sous forme d'une simple chaîne polypeptidique. Dans l'organisme, il est libéré de manière pulsatile toutes les 3-4 heures environ, avec des concentrations maximales observées la nuit. Le processus de sécrétion de l'hormone est régulé par des hormones hypothalamiques aux effets opposés. Ces hormones comprennent l'hormone libérant l'hormone de croissance GN-RH et l'hormone inhibant sa libération SRIF. Lors de la libération de la somatotropine, ce processus est régulé par des neurohormones : somatolibérine (GHRH), somatostatine (GHIH), ghréline, glucocorticoïdes, acides gras, glucose, insuline et hormones sexuelles. L'hormone de croissance régule les processus métaboliques, la modulation de la croissance de l'organisme, la stimulation et la prolifération cellulaire. L'action du HGH est assez large et comprend notamment la stimulation de la croissance des os longs, la synthèse des acides nucléiques, la régulation du métabolisme des glucides. L'hormone de croissance a une large application chez les sportifs. L'administration de somatotropine chez les sportifs favorise le renforcement, la construction musculaire ainsi que la minimisation des blessures pendant les entraînements, grâce au développement du tissu conjonctif qui forme le cartilage. Lors de la décision de prendre l'hormone de croissance, il est important de maintenir également d'autres facteurs tels qu'une quantité suffisante de sommeil ou une alimentation appropriée. Rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme
Conclusions
Comme mentionné ci-dessus, les acides aminés, les protéines et les peptides participent au bon fonctionnement de l'organisme. En ce qui concerne les peptides, on peut en déduire qu'une utilisation habile permet une thérapie de santé sûre, efficace et satisfaisante. Compte tenu de leur action, ils sont recommandés dans presque tous les cas et pour toutes les personnes. Ils sont particulièrement conseillés aux sportifs à des fins de régénération et de prévention. Les carences en hormones protéiques ainsi qu'en hormones peptidiques peuvent entraîner de graves troubles du fonctionnement de l'organisme. Rôle biologique des acides aminés, des protéines et des peptides dans le bon fonctionnement et la régénération de l'organisme.
Bibliographie:
- Bańkowski.E, Biochimie. 2020; 160(1-3):33-41
- Dryweń.M, Dźwigała J, Importance des acides aminés à chaîne ramifiée dans la nutrition humaine ainsi que dans la prévention et le déroulement de certaines maladies. Médecine Générale et Sciences de la Santé; 2013; 3(1) 379-384
- Darewicz.M, Borawska J, Minkiewicz P, Peptides biologiquement actifs libérés à partir des protéines alimentaires. 2015; 3(100) 26-41; DOI:10.15193/zntj/2015/100/037
- Miyamoto.T, Détection et quantification des résidus d'acides aminés D dans les peptides et protéines par hydrolyse acide. 2018; 775-782; DOI:10.1016/j.bbapap.2017.12.010
- Bottecchia.C, Modification photocatalytique des acides aminés, peptides et protéines. 2018; 26-42; DOI:10.1002/chem.201803074
- Rutherfurd M, Analyse des acides aminés. 2009; 11.9.1-11.9.37; DOI:10.1002/0471140864.ps1109s58
- Rob.M, Liskamp.J, Peptides et protéines comme source continue et passionnante d'inspiration pour les peptidomimétiques. 2011; 1626-1653; DOI:10.1002/cbic.201000717
- Lewandowski K, Lewiński A, Hormones peptidiques sécrétées dans le tube digestif. 2012: 12(1) 10-14
- Klein A. Mécanismes moléculaires de la régulation hormonale. Éditions de l'Université Jagellonne. 2010; 200-233
- Marciniak. P, Szymczak.M, Hormones peptidiques. Progrès en biologie cellulaire. 2011; 43-63
- O’Neill.R, Murphy.R, Endocrinologie. 2012; 30-45
- Siewko.K, Szelachowska.M, Peptide C comme facteur de risque de développement du diabète de type 1 chez les parents au premier degré de personnes atteintes de diabète auto-immun. P2009; 60(5) 26-43
- Romański.K, Goździewska.K, Ghréline et motiline : similitudes et différences dans la régulation de l'activité motrice du tube digestif. 2008; 64(11) 5-19
- Nylec.M, Olszanecka.M, Rôle du glucagon dans la pathogenèse du diabète de type II. 2010; 1734-3321
- Hsiao.Y, Yamada.M, Rôles des hormones peptidiques et de leurs récepteurs lors du développement des racines des plantes. 2020; 12(1) 22; DOI:10.3390/genes12010022
- Imura.H, Nakai Y, Tanaka N, ACTH et peptides apparentés. 2000; 41(5) 949-56
- Brownstein M, Hormone adrénocorticotrope dans le système nerveux central. 2000; 22: 93-9
- Itoh. A, Motiline et application clinique. 2001; 593-608; DOI:10.1016/S0196-9781(96)00333-6 19. Chen.C, Ghréline et motiline dans le système gastro-intestinal. 2012; DOI:10.2174/138161212803216915
- Drucker.D, Mécanismes d'action et application thérapeutique du peptide-1 de type glucagon. Métabolisme cellulaire, 2018: 740-756; DOI:10.1016/j.cmet.2018.03.001
- Bildingmaier. M, Hormone de croissance. 2009; 187-200
- Lee.S, Park.H, Évaluation de la bio-efficacité d'une forme stabilisée d'hormone de croissance humaine (SP-hGH). 2013; 45(10):722 -727; DOI:10.1055/s-0033-1345126
- Maciejewska.Z, Korek.E, Rôle de l'hormone de croissance, du facteur de croissance insulinomimétique de type 1 et de la ghréline. 2016; 216-220





BPC-157 Produit de l'année 2020 ! L'innovation en première place !
Action neuroprotectrice et antidépresseur du BPC-157. Influence du BPC-157 sur le fonctionnement du cerveau.