Mots-clés : peptide ; hydrolyse peptidique ; liaisons peptidiques ; modifications peptidiques, synthèse peptidique ; liaison peptidique ; hormones peptidiques ; analogues peptidiques ; salification ; amidation ; acétylation
Peptides
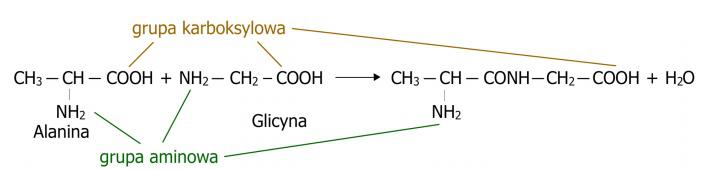
Les peptides sont des composés chimiques construits de manière similaire aux protéines, à partir d’acides aminés. Ils se forment par la liaison de deux acides aminés ou plus via une liaison peptidique lors d’un processus de condensation, où, en plus du peptide, une molécule d’eau est également produite. (Fig.1) Ils suscitent un large intérêt en raison de leurs fonctions biologiques importantes. De nombreuses hormones ainsi que des neurotransmetteurs sont précisément des peptides. Dans le cas des peptides endogènes, ils agissent comme agents antimicrobiens, jouant un rôle de système de défense de l’organisme. Les peptides naturellement présents ainsi que leurs analogues synthétiques sont considérés comme des composés attrayants d’un point de vue thérapeutique en raison de leur haute activité, faible toxicité et absence d’interactions médicamenteuses. En pratique médicale, seuls quelques peptides sont utilisés en raison de leur instabilité biologique et de leur dégradation rapide, mais la synthèse peptidique permet d’obtenir des formes stables. C’est également le cas, par exemple, pour la synthèse de peptides à partir de sources naturelles. Les peptides existent sous une forme non ramifiée, possédant seulement deux extrémités spécifiques. L’une est appelée extrémité aminée, où se trouve un acide aminé avec un groupe α-amine libre. L’autre est appelée extrémité carboxyle ou extrémité C, où se trouve un acide aminé avec un groupe α-carboxyle libre.
Nomenclature des peptides
La nomenclature des peptides commence par le nom du résidu d’acide aminé à l’extrémité N, puis énumère les noms des résidus d’acides aminés suivants, et se termine par le nom de l’acide aminé à l’extrémité C. L’ordre des acides aminés est noté à l’aide de symboles à trois lettres ou à une lettre.
Liaison peptidique
Le carbone, à la suite de la réaction du groupe α-carboxyle, se lie à l’azote du groupe α-amine par une liaison simple, la liaison peptidique. On considère généralement que cette liaison existe sous deux formes structurelles qui restent en équilibre mutuel défini. La liaison C-N passe en C=N et inversement. La rotation autour de l’axe C=N n’est pas possible, ce qui rend la liaison peptidique suffisamment rigide pour posséder les caractéristiques d’une double liaison. Dans le cas de la liaison peptidique impliquant le groupe imine de la proline ou de l’hydroxyproline avec le groupe carboxyle d’un autre acide aminé, une structure distincte se forme. L’azote est alors intégré dans la structure du cycle pyrrolidine, il n’y a pas de substituant hydrogène, ce qui empêche la rotation autour des liaisons impliquant cet azote. Les acides aminés participant à la formation de la liaison peptidique perdent des fragments moléculaires : ce sont des molécules -OH du groupe carboxyle et -H du groupe amine. C’est pourquoi les acides aminés présents dans les peptides et les protéines sont appelés résidus d’acides aminés. Les liaisons peptidiques formées sont stables et leur rupture ne peut se produire qu’en présence de bases ou d’acides forts à haute température.
Rupture de la liaison peptidique
La rupture de la liaison peptidique se produit par une réaction d’hydrolyse du peptide, qui consiste à rompre les liaisons peptidiques formées et à reconstituer les acides aminés individuels. Cette réaction implique de l’eau, dont les molécules se décomposent en groupes hydroxyles (-OH) et atomes d’hydrogène (H), qui se lient ensuite aux liaisons libérées des substances.
Classification des peptides
La classification des peptides est établie en fonction du nombre d’acides aminés qui les composent. Dans la classification générale des peptides, on distingue :
-
Les dipeptides – produits résultant de la réaction de deux acides aminés, avec un groupe amine libre sur l’un et un groupe carboxyle libre sur l’autre ;
-
Les oligopeptides – peptides composés de quelques à une douzaine d’acides aminés ;
-
Les polypeptides – peptides plus longs, contenant plusieurs dizaines de résidus d’acides aminés ;
-
Les protéines – considérées comme telles lorsque la molécule contient plus de cent résidus d’acides aminés.
Spectrum d’activité des peptides
Les peptides présentent un large spectre d’activité biologique et sont utilisés dans le traitement des infections bactériennes, des maladies virales, des affections du système cardiovasculaire, du système osseux, du système nerveux, du diabète ou de l’ostéoporose.
Avantages des peptides
- Haute activité et sélectivité
- Large éventail de cibles moléculaires
- Potentiellement moins toxiques que les composés de faible poids moléculaire
- Faible accumulation dans les tissus
- Grande diversité chimique et biologique
- Possibilité de découverte au niveau génétique
- Synthèse facile des analogues
Synthèse des peptides
Selon le peptide que l’on souhaite obtenir, une méthode de synthèse appropriée est nécessaire. En bref, nous allons présenter la synthèse des peptides en fonction de leur taille. Pour obtenir un dipeptide, il faut utiliser un réactif qui active le groupe carboxyle de l’acide aminé arylant ou convertir l’acide aminé acylant en anhydride. La synthèse des peptides plus grands, obtenus à partir du dipeptide, est un processus plus laborieux et complexe, impliquant la suppression de la protection du groupe amine de l’acide aminé N-terminal et son acylation par un autre acide aminé N-protégé. Ce processus est particulièrement long car ces étapes sont répétées jusqu’à l’obtention du peptide avec la séquence désirée. Pour la synthèse de peptides de grande taille, la méthode de Merrifield est la plus efficace et la plus simple. Cette méthode est réalisée en phase solide. L’acide aminé C-terminal est fixé à un polymère, puis les acides aminés suivants sont ajoutés un à un jusqu’à atteindre la longueur de chaîne souhaitée.
Peptides biologiquement actifs
Les hormones peptidiques et protéiques sont couramment présentes dans notre environnement. Elles étaient auparavant connues principalement comme des formes peu stables. Grâce à la synthèse, il est désormais possible de concevoir des thérapies peptidiques durables et efficaces selon les besoins de l’organisme. C’est pourquoi il est important de manipuler habilement et en toute sécurité la stimulation hormonale. Parmi les peptides biologiquement actifs, on peut citer le glutathion, un tripeptide à structure spécifique composé de glutamate, cystéine et glycine. Le glutamate est l’acide aminé N-terminal. La liaison entre le glutamate et la cystéine est cependant atypique pour les peptides et protéines, car ce n’est pas le groupe α-carboxyle du glutamate qui est impliqué, mais le groupe γ-carboxyle. Le glutathion existe donc sous forme réduite et oxydée, en tant que γ-glutamylcystéinylglycine. Sous forme réduite, il possède un groupe sulfhydryle libre, tandis que sous forme oxydée, une paire d’atomes d’hydrogène est détachée des groupes –SH. Les atomes de soufre restent sans hydrogène, ce qui conduit à la formation d’un pont disulfure. La capacité du glutathion à se modifier en forme oxydée ou réduite est importante dans les processus d’oxydoréduction.
Un autre exemple est l’ocytocine et la vasopressine, qui sont des nanopeptides produits par les neurones de l’hypothalamus et libérés par la posthypophyse, ne différant que par deux acides aminés. La cystéine se trouve en deux positions, ce qui conduit à la formation d’un pont disulfure. L’ocytocine agit comme une hormone stimulant les contractions utérines. La vasopressine stimule la réabsorption d’eau dans les tubules rénaux. Elle joue également un rôle important dans la régulation de la sécrétion de l’hormone adrénocorticotrope (ACTH) en situation de stress.
Hormones peptidiques
Hormone adrénocorticotrope (ACTH)
L’hormone adrénocorticotrope, peptide de 39 acides aminés, est produite par la dégradation d’une molécule précurseur beaucoup plus grande, la pro-opiomélanocortine (POMC). La pro-opiomélanocortine est également la source d’autres peptides actifs. Deux peptides sont contenus dans la structure de l’ACTH : l’hormone α-mélanotropique (α-MSH), identique aux 13 premiers acides aminés de l’ACTH, et un peptide de la partie intermédiaire de l’hypophyse, similaire à la corticotropine – fragment 18-39 de l’ACTH. La fonction principale de l’ACTH est de stimuler le cortex surrénalien afin qu’il puisse sécréter des hormones stéroïdes. L’ACTH régule l’activité des couches fasciculée et réticulée du cortex. Les 18 premiers acides aminés sont responsables de l’activité biologique de l’ACTH. La régulation de l’ACTH est assurée par la corticolibérine (CRH), une hormone de l’hypothalamus, qui libère la corticotropine via un rétrocontrôle négatif par le cortisol. Cela signifie qu’un déficit en cortisol stimule la production de CRH et d’ACTH, tandis qu’un excès inhibe leur sécrétion. La libération de cortisol régule ainsi de nombreuses fonctions vitales, notamment la mobilisation de l’organisme en situation de stress, l’augmentation de la pression artérielle et les capacités anti-inflammatoires. L’ACTH est sécrété de manière pulsatile selon un rythme circadien, avec une concentration maximale le matin, moment où elle est le plus nécessaire, puis décroissant au cours de la journée. Une augmentation de la sécrétion d’ACTH est observée dans des pathologies telles que l’insuffisance corticosurrénalienne, la maladie de Cushing ou le syndrome de Nelson.
Insuline et peptide C
L’insuline et le peptide C sont sécrétés en continu par le pancréas humain. Lors de la biosynthèse de l’insuline, le peptide C est produit. Les cellules pancréatiques produisent d’abord la préproinsuline, qui subit des modifications par élimination d’acides aminés pour former la proinsuline, composée de deux chaînes A et B reliées par le peptide C. Ensuite, le peptide C est détaché de la proinsuline, formant la forme finale de l’insuline. Lorsqu’il y a du glucose dans l’organisme, le pancréas reçoit le signal de libérer les granules contenant l’insuline et le peptide C. Le peptide C est maintenu dans le foie beaucoup plus longtemps que l’insuline, car il n’y est pas dégradé. Sa dégradation a lieu principalement dans les reins. Des concentrations trop élevées ou trop basses d’insuline ou de peptide C peuvent conduire au développement du diabète de type I ou II ainsi qu’à la maladie de Cushing. Les fluctuations du peptide C peuvent également indiquer une insuffisance rénale chronique ou la présence de métastases ou de récidives locales de tumeur, ce qui rend le maintien de leurs concentrations normales très important.
Motiline
La motiline est une hormone liée aux muscles lisses de l’estomac et des intestins, contrôlée par les fibres du nerf vague. Elle est synthétisée dans les cellules endocrines. En tant qu’hormone peptidique composée de 22 acides aminés dans une séquence spécifique, elle est produite par les cellules de l’intestin grêle. Produite par les cellules endocrines du système digestif M (Mo), elle participe à la régulation de la motilité gastro-intestinale. La motiline est une hormone importante impliquée dans la phase III du complexe moteur migrant (MMC), durant laquelle l’estomac et l’intestin grêle doivent vider l’estomac des résidus alimentaires inutiles et des cellules épithéliales desquammées, en stimulant les mouvements péristaltiques. Cette hormone influence également la vidange de la vésicule biliaire pendant la période inter-digestive, lorsque la concentration de motiline est la plus élevée.
Glucagon
Le glucagon est une des hormones impliquées dans la régulation de la concentration de glucose. Ce peptide est sécrété par les cellules endocrines du pancréas. C’est un polypeptide composé de 29 acides aminés, issu d’un précurseur de 180 acides aminés. Les variations de la concentration de glucose stimulent la sécrétion de glucagon. La production de cette hormone a lieu dans les îlots pancréatiques, où le proglucagon donne naissance au glucagon ainsi qu’au polypeptide pancréatique dépendant de la glicentine (GRPP). La fonction principale du glucagon est de maintenir une concentration normale de glucose dans le sérum lors de sa baisse entre les repas ou pendant l’effort physique. Ses réserves sont alors libérées par le foie pour assurer une protection adéquate de l’organisme. De plus, il peut participer à la régulation de la prise alimentaire, ce qui peut entraîner une sensation de satiété plus précoce. Le glucagon peut potentiellement inhiber la libération de ghréline et également freiner la motilité intestinale.
Analogues peptidiques
Les analogues peptidiques sont des composés chimiques dans lesquels un atome est remplacé par un autre par rapport au composé d’origine. La structure générale du peptide reste inchangée. Les analogues peptidiques comprennent les analogues en hélice ainsi que les analogues de coudes β et de feuillets β. Dans les premiers, les hélices sont un des éléments structurels clés des peptides bioactifs. La stabilisation de courts fragments d’oligomères en conformation hélicoïdale augmente leur activité. Dans les analogues de coudes β et de feuillets β, des résidus d’acides aminés D ou β, γ, δ sont insérés. Les analogues peptidiques permettent d’obtenir de nouveaux composés peptidiques plus stables, utilisables dans un spectre plus large de symptômes et ouvrant la voie à des solutions innovantes aux problèmes liés aux formes préexistantes.
Salification des peptides
Le processus de salification consiste à modifier les charges des protéines. Les charges des protéines sont neutralisées par les anions et cations des sels. Les molécules de protéines ne s’attirent plus et ne forment pas d’agrégats, et la protéine est précipitée en raison de la perte de son manteau d’eau. Ce processus est réversible. L’inverse consiste à éliminer le sel par dialyse ou à réduire sa concentration en ajoutant de l’eau. Sur la base de nos articles précédents, on peut affirmer que la salification ayant conduit à la formation d’une forme stable du peptide BPC-157 est une méthode innovante pour assurer la stabilité peptidique et ainsi étendre l’action biologique des peptides.
Acétylation des peptides
L’acétylation consiste à ajouter des radicaux acétyle aux substrats, qui sont des composés avec un groupe NH2, OH ou SH, en présence de l’enzyme N-acétyltransférase. La source du radical acétyle est l’acétyl-CoA. La fonction principale des N-acétyltransférases est de faciliter la liaison du groupe acétyle au groupe amine des amines aromatiques et des hydrazines (réaction d’acétylation N), c’est-à-dire la détoxification de composés exogènes potentiellement toxiques.
Amidation des peptides
Lorsqu’il y a rupture des liaisons peptidiques et fragmentation de la chaîne polypeptidique, des groupes carbonyles se forment. L’oxydation de la molécule protéique par un radical hydroxyle commence par le détachement d’un atome d’hydrogène au carbone α de l’acide aminé. Le radical alkyle formé réagit avec l’oxygène pour former un radical alkylperoxyle qui se transforme en hydroperoxyde alkyle. Le radical alkoxyle qui en résulte peut se transformer en résidu aminé hydroxylé au carbone α ou provoquer la fragmentation de la chaîne polypeptidique. La présence du radical alkoxyle favorise la fragmentation de la chaîne polypeptidique. La rupture de la liaison peptidique peut se produire par amidation α ou diamidation. Lors de la fragmentation α-amidique, le peptide N-terminal possède un groupe amide à l’extrémité C, tandis que l’autre peptide contient à l’extrémité N un dérivé N-α-cétoacyle. La fragmentation par diamidation se caractérise par la formation d’un peptide N-terminal avec une structure diamide et d’un peptide provenant de l’extrémité C de la protéine contenant à l’extrémité N une structure isocyanate.
Bibliographie 1. Murray R. K., Granner D. K., Mayes P. A., Rodwell V, Biochimie Harper. 1995 ; Éditions Médicales PZWL
2. Jakubke H. D., Jeschkeit H, Acides aminés peptides protéines. 1982 ; Éditions Scientifiques d’État
3. Kołodziejczak A, Acides aminés et peptides. 2006





L'impact de la thérapie BPC-157 sur le système immunitaire
Peptides aux propriétés antimicrobiennes et leurs analogues obtenus par modification.