Los aminoácidos con diferentes longitudes de cadena y secuencias pueden formar dímeros y polímeros. Dependiendo del número de residuos de aminoácidos localizados en la cadena polimérica, los polímeros se dividen en péptidos y proteínas. Los péptidos contienen en su estructura alrededor de 50 aminoácidos y las proteínas contienen en una o varias cadenas un número mayor de residuos de aminoácidos que los péptidos. Tanto los aminoácidos, proteínas y péptidos juegan un papel importante en el correcto funcionamiento del organismo. Gracias a las terapias peptídicas modernas, es posible permitir la regeneración del organismo.
Palabras clave: péptido · aminoácido · proteína · hélice α · estructura β · cadena no polar · alanina · valina · leucina · isoleucina · fenilalanina · triptófano · metionina · prolina · glicina · serina · treonina · tirosina · cisteína · asparagina · glutamina · ácido aspártico · ácido glutámico · configuración · conformación · dipéptido · oligopeptídico · enlace peptídico · hormona de crecimiento
Lista de abreviaturas: ACTH- adrenocorticotropina; CRH- corticoliberina; POMC- proopiomelanocortina; MMC- complejo motor migratorio; GRPP- polipéptido pancreático dependiente de glicentina; HGH- hormona de crecimiento. El papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo se presenta a continuación para familiarizarse con su acción y las posibilidades que ofrecen.
Características de los aminoácidos
Los aminoácidos, como uno de los componentes mejor conocidos de los organismos vivos, se presentan como derivados de ácidos orgánicos, donde al menos uno de los átomos de hidrógeno es reemplazado por un grupo amino. Son componentes que se encuentran comúnmente tanto en forma libre como ligada, en el caso de los péptidos o proteínas. Cada uno de los aminoácidos que se encuentran en las proteínas, con excepción de la prolina y la hidroxiprolina, posee un grupo amino ubicado en el carbono α y una cadena lateral R, que puede tener una estructura variable y está unida al mismo átomo de carbono.
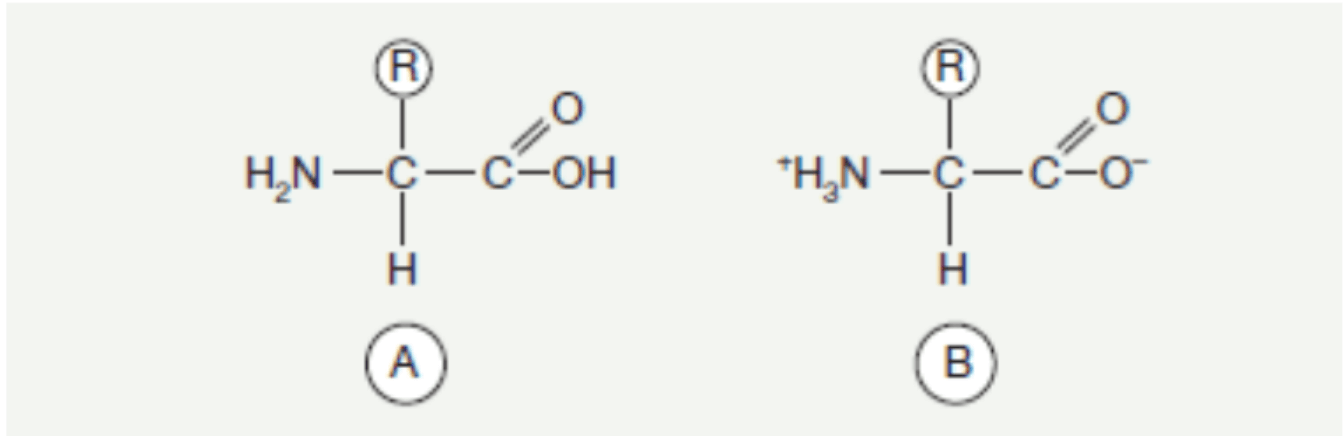
Fórmula general del aminoácido.
A. En forma libre
B. En forma de ion zwitteriónico. En el medio se conocen alrededor de 300 aminoácidos, pero los que aparecen comúnmente son 22, de los cuales 2 adicionales se han descubierto relativamente hace poco y solo se encuentran en algunas proteínas. La presencia y ubicación en la estructura de la proteína de los aminoácidos ya conocidos está determinada por propiedades genéticas; en algunos casos, es resultado de modificaciones postraduccionales de los residuos de aminoácidos que previamente fueron incorporados a la cadena proteica. Los demás aminoácidos pueden existir en forma libre o en compuestos no proteicos. La función del aminoácido en la proteína está determinada por la estructura de su cadena lateral, por lo que la clasificación de los aminoácidos se define en varios grupos, según el carácter de las cadenas laterales que posee el aminoácido.
Aminoácidos con cadenas no polares
Al grupo de aminoácidos con cadenas no polares pertenecen, en orden: alanina, valina, leucina, isoleucina, fenilalanina, triptófano, metionina, prolina y glicina. En el caso de los dos últimos aminoácidos mencionados, existe cierta relación. La prolina, como ejemplo atípico, no posee un grupo α-amino sino un grupo imino, que está incorporado en la estructura del anillo de pirrolidina. Papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo. La glicina, por su parte, no tiene cadena lateral, siendo reemplazada por un átomo de hidrógeno. Cada uno de los aminoácidos mencionados posee una cadena lateral no polar, que no tiene capacidad para captar o perder protones y no participa en la formación de enlaces de hidrógeno o iónicos. La cadena lateral se considera generalmente lipofílica, es decir, hidrofóbica—no unida al agua. Estas cadenas evitan el ambiente acuoso al adherirse entre sí y se orientan hacia el interior de la molécula proteica. Cuando están en un medio acuoso, su comportamiento se puede comparar mejor con el de gotas de aceite, que se unen en gotas más grandes, reduciendo así el contacto con el agua.
Aminoácidos con cadenas laterales polares sin carga
Al grupo de aminoácidos con cadenas laterales polares sin carga pertenecen: serina, treonina, tirosina, cisteína, asparagina y glutamina. Estos aminoácidos tienen carga cero en un ambiente de pH neutro, aunque en el caso de la cisteína y la tirosina, a pH básico, pueden perder un protón. La serina, treonina y tirosina pueden formar enlaces de hidrógeno debido a la presencia de un grupo hidroxilo polar. También en las cadenas laterales de la asparagina y glutamina pueden formarse enlaces de hidrógeno debido a la presencia de grupos carbonilo y amida. El grupo amida de la asparagina, así como los grupos hidroxilo de la serina y treonina, pueden ser sitios de unión para componentes azucarados. Papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo.
Aminoácidos con cadenas ácidas
Al grupo de aminoácidos con cadenas ácidas pertenecen el ácido aspártico y el ácido glutámico. En la estructura de las cadenas laterales de estos aminoácidos se observan grupos carboxilo. En un ambiente de pH neutro, estos grupos se disocian completamente, convirtiéndose en portadores de carga negativa. Las formas completamente ionizadas del ácido aspártico y del ácido glutámico se denominan aspartato y glutamato, respectivamente. Los nombres transformados, tras la ionización, indican que en un ambiente con pH fisiológico son aniones. Papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo
Aminoácidos con cadenas básicas
Aminoácidos con cadenas básicas. Al grupo de aminoácidos con cadenas básicas pertenecen: lisina, arginina e histidina. Las cadenas laterales de estos aminoácidos contienen grupos capaces de unir protones. Estos grupos incluyen el grupo ε-amino de la lisina, el grupo guanidino de la arginina y el anillo imidazol de la histidina. A pH fisiológico, los grupos R de la lisina y la arginina están completamente ionizados, lo que les confiere una carga positiva. El aminoácido libre histidina tiene un carácter ligeramente básico y se encuentra en forma neutra a pH fisiológico. Sin embargo, puede ocurrir que la histidina en una proteína tenga un grupo R cargado positivamente o neutro, dependiendo del ambiente que genere la proteína. Esto juega un papel importante en la función de la proteína hemoglobina.
Proteínas
Características de las proteínas
Las proteínas, como polímeros condensados de aminoácidos que se encuentran abundantemente en el cuerpo humano, son un componente estructural fundamental para su correcto funcionamiento. Construidas exclusivamente a partir de residuos de aminoácidos, se denominan proteínas simples o proteínas. Las proteínas complejas, proteidas, contienen además un grupo prostético que no es un componente proteico. Como productos macromoleculares, se forman mediante la interacción del grupo α-carboxilo de un aminoácido con el grupo α-amino de otro aminoácido, formando un enlace peptídico. Podemos llamar polipéptidos a las proteínas cuya masa molecular es mayor a 10,000 daltons (Da). Todas las proteínas con masa molecular inferior se denominan oligopeptidos. Cada proteína posee una cadena proteica compuesta por entre 100 y 1000 residuos de aminoácidos.
Estructura primaria
La estructura primaria de la cadena polipeptídica de una proteína dada determina el orden (secuencia) de la unión de los residuos de aminoácidos en la cadena polipeptídica. Los aminoácidos individuales están unidos covalentemente mediante enlaces peptídicos. En las proteínas solo existen secuencias específicas de aminoácidos debido a la gran posibilidad de combinaciones. La disposición de los residuos de aminoácidos a lo largo de la cadena polipeptídica no está estricta ni claramente definida. En el ejemplo de la molécula de proteína que es la hemoglobina, se puede señalar la importancia de la estructura primaria. En este caso, la sustitución de un aminoácido por otro provoca la formación de hemoglobina patológica. Para entender mejor la esencia de su formación, por ejemplo, en la posición sexta, el glutamato es reemplazado por otro aminoácido (valina o lisina), lo que conduce a consecuencias biológicas negativas. Los glóbulos rojos pasan a un estado biológicamente alterado, lo que provoca un cambio en la forma de los glóbulos rojos a una forma atípica. Los glóbulos se vuelven susceptibles a la hemólisis, lo que a su vez causa una disminución en el número de eritrocitos en la sangre. Los productos de descomposición de los eritrocitos son captados por el hígado y el bazo, y la concentración del pigmento biliar, es decir, la bilirrubina, aumenta como resultado de la descomposición del hemo en la hemoglobina. La consecuencia de estos procesos es el desarrollo de una condición patológica llamada anemia hemolítica.
Estructura secundaria
Hablando de la estructura secundaria, los términos básicos son configuración y conformación. Mientras que la configuración se refiere a las relaciones geométricas entre conjuntos específicos de átomos, la conformación se refiere a la estructura espacial de la proteína. En el caso de la configuración, se produce un cambio mutuo en la construcción de enlaces ya formados, por ejemplo, la transformación de D-alanina en L-arginina. Esta conversión se puede lograr rompiendo los enlaces covalentes existentes y formándolos de nuevo. La conformación, en cambio, no conduce a la ruptura de enlaces covalentes, sino a la ruptura y reformación de fuerzas no covalentes, como puentes de hidrógeno o interacciones hidrofóbicas. Solo algunas conformaciones resultantes tienen importancia biológica. La forma más común de la estructura secundaria de la proteína es la hélice α en forma de espiral. Cada vuelta de la hélice α corresponde a 3,6 residuos de aminoácidos. El papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo. La forma específica y diferente de espiral permite la formación de puentes de hidrógeno, tanto intra-cadena como interhélice, con máxima fuerza debido a la posibilidad de interacciones electrostáticas. La estructura de la hélice α, que incluye el enlace peptídico de la cadena proteica, permite su participación en la formación de puentes de hidrógeno, excepto aquellos que involucran grupos imino de la prolina. Los polipéptidos obtenidos mediante síntesis a partir de L-aminoácidos o D-aminoácidos forman espontáneamente la estructura de hélice α. En el caso de polipéptidos formados a partir de racematos de aminoácidos y polímeros de algunos aminoácidos, como la prolina o la hidroxiprolina, no tienen la capacidad de formarla espontáneamente. Por ejemplo, la α-queratina, que es una proteína presente, entre otros, en el cabello y está casi completamente formada por estructura de hélice α, mientras que el colágeno o la elastina, que contienen prolina e hidroxiprolina, no tienen ninguna capacidad para formar esta estructura.
Estructura terciaria
La estructura terciaria permite mantener la estructura secundaria mediante el plegamiento tridimensional de la molécula proteica. El papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo. La estructura primaria es principalmente responsable del empaquetamiento espacial de la molécula proteica, y de forma indirecta también la secundaria. La estructura terciaria se estabiliza por interacciones entre las cadenas laterales de los residuos de aminoácidos, incluyendo enlaces covalentes, en este caso puentes de hidrógeno, así como enlaces no covalentes de baja energía, es decir, enlaces de hidrógeno. En soluciones acuosas, la estructura de las proteínas globulares es compacta. Las cadenas laterales hidrofóbicas de los residuos de aminoácidos están ocultas dentro de la molécula, mientras que los grupos hidrofílicos se encuentran en la superficie. Los grupos polares, incluidos los ocultos en el interior de la molécula junto con los componentes de los enlaces peptídicos, permiten la formación de enlaces de hidrógeno y de interacciones electrostáticas. La estructura terciaria solo se forma cuando existen enlaces que permiten la unión de residuos de aminoácidos linealmente distantes.
Estructura cuaternaria
La última de las estructuras presentadas ocurre solo en algunas proteínas y determina la disposición espacial y la composición de subunidades en relación con una molécula proteica. En este caso, las proteínas tienen un alto peso molecular y están formadas por dos o más monómeros, es decir, cadenas peptídicas. Generalmente, en la estructura cuaternaria, los elementos proteicos que participan en su formación están unidos por enlaces de hidrógeno de baja energía. En algunos casos, la estructura se estabiliza mediante puentes disulfuro entre residuos de cisteína. En el caso del colágeno y la elastina, los enlaces covalentes entre subunidades son excepcionalmente estables. Las propiedades biológicas de la estructura cuaternaria pueden ser modificadas por sustancias de bajo peso molecular conocidas como efectores alostéricos. En el caso de la hemoglobina y las proteínas enzimáticas, especialmente la deshidrogenasa láctica, la estructura cuaternaria está muy bien estudiada. El papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo.
Péptidos
Características de los péptidos
Los péptidos son compuestos químicos construidos de manera similar a las proteínas, a partir de aminoácidos. Son objeto de amplio interés, desempeñando funciones biológicas importantes. Muchos hormonas y neurotransmisores son precisamente péptidos. En el caso de los péptidos endógenos, actúan contra microorganismos, funcionando como un sistema de defensa del organismo. Los péptidos que ocurren de forma natural y sus análogos sintéticos son considerados compuestos atractivos con importancia terapéutica debido a su alto grado de actividad, baja toxicidad y ausencia de interacciones con medicamentos. En la práctica médica, solo unos pocos péptidos se utilizan debido a su inestabilidad biológica y rápida degradación, sin embargo, la síntesis de péptidos permite obtener formas estables. De manera similar ocurre, por ejemplo, con la síntesis de péptidos a partir de fuentes naturales, que se utilizan, entre otras cosas, para la producción de vacunas. El producto que resulta de la reacción de dos aminoácidos se llama dipéptido, manteniendo un grupo amino libre de uno de los aminoácidos y un grupo carboxilo libre del otro aminoácido. Los péptidos que están compuestos por varios hasta una docena de aminoácidos se denominan oligopeptidos, mientras que los péptidos más largos, que contienen varias decenas de residuos de aminoácidos, se llaman polipéptidos. La nomenclatura de los péptidos comienza con el nombre del residuo de aminoácido N-terminal, luego se enumeran los nombres de los residuos de aminoácidos siguientes y termina con el nombre del aminoácido C-terminal. La secuencia de aminoácidos se escribe usando símbolos de tres letras o de una letra. Los péptidos existen en forma no ramificada, con solo dos extremos específicos. Uno de ellos se llama extremo amino, donde se encuentra el aminoácido con un grupo α-amino libre. El otro se llama extremo carboxilo o extremo C, donde se encuentra el aminoácido con un grupo α-carboxilo libre.
Enlace peptídico
El carbono, como resultado de la reacción del grupo α-carboxilo, se une al nitrógeno del grupo α-amino mediante un enlace simple, el enlace peptídico. Se supone que este enlace existe en forma de dos estructuras que permanecen en un equilibrio mutuo definido. El enlace C-N se convierte en C=N y viceversa. La rotación alrededor del eje C=N no es posible, por lo que el enlace peptídico es lo suficientemente rígido como para tener características de un enlace doble. El papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo 9 En el caso del enlace peptídico que involucra el grupo imino de la prolina o hidroxiprolina con el grupo carboxilo de otro aminoácido, se forma una estructura diferente y separada. El nitrógeno en este caso está incorporado en la estructura del anillo de pirrolidina, no hay un sustituyente de hidrógeno, por lo que no hay posibilidad de rotación alrededor de los enlaces que se forman en presencia de nitrógeno. Los aminoácidos que participan en la formación del enlace peptídico pierden fragmentos de moléculas. Son moléculas -OH del grupo carboxilo y -H del grupo amino. Por eso, los aminoácidos que se encuentran en péptidos y proteínas se llaman residuos de aminoácidos. Los enlaces peptídicos formados son estables y su ruptura solo puede ocurrir bajo la acción de bases y ácidos fuertes a la vez que a alta temperatura.
Péptidos biológicamente activos
Las hormonas peptídicas y las hormonas proteicas son comunes en el entorno que nos rodea. Anteriormente se conocían en su mayoría como formas poco estables. Bajo la influencia de la síntesis, cada vez es más posible seleccionar una terapia peptídica que sea duradera y eficaz según las necesidades del organismo. Por eso vale la pena manejar con habilidad y seguridad la estimulación hormonal. Considerando algunos péptidos biológicamente activos, podemos poner como ejemplo al glutatión, que siendo un tripéptido con una estructura específica está compuesto por glutamato, cisteína y glicina. El glutamato aparece como aminoácido N-terminal. La unión del glutamato con la cisteína es inusual para péptidos y proteínas, ya que aquí no está presente el grupo α-carboxilo del glutamato, sino el grupo γ-carboxilo. Por lo tanto, el glutatión existe en forma reducida y oxidada, siendo γ-glutamilcisteinilglicina. En su forma reducida posee un grupo sulfhidrilo libre y en la forma oxidada se produce la separación de un par de átomos de hidrógeno de los grupos –SH. Los átomos de azufre quedan sin hidrógeno, lo que da lugar a la formación de un puente disulfuro. La capacidad modificadora del glutatión en estado oxidado o reducido es importante en los procesos redox. Otro ejemplo son la oxitocina y la vasopresina, que siendo nano-péptidos producidos por las neuronas del hipotálamo y liberados por el lóbulo posterior de la hipófisis, solo difieren en dos aminoácidos. La cisteína está en dos posiciones, lo que conduce a la formación de un puente disulfuro. La oxitocina actúa como hormona que estimula las contracciones uterinas. La vasopresina, en cambio, estimula la reabsorción de agua en los túbulos renales. La vasopresina también juega un papel importante en la regulación de la secreción de la hormona adrenocorticotrópica (ACTH) en situaciones de estrés. El papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo.
Hormonas peptídicas
Hormona adrenocorticotrópica (ACTH)
La hormona adrenocorticotrópica, un péptido de 39 aminoácidos, se produce por la degradación de una molécula precursora mucho mayor llamada proopiomelanocortina (POMC). La proopiomelanocortina también es fuente de otros péptidos activos. Dos péptidos están contenidos en la estructura de la ACTH. Estos incluyen la hormona α-melanotropina (α-MSH), que es idéntica en estructura a los primeros 13 aminoácidos de la ACTH, y el péptido de la parte intermedia de la hipófisis similar a la corticotropina, fragmento 18-39 de la ACTH. La función principal de la ACTH es estimular la corteza suprarrenal para que pueda secretar hormonas esteroides. La hormona adrenocorticotrópica regula la actividad en las capas fasciculada y reticular. La actividad biológica de la ACTH depende de los primeros 18 aminoácidos. La regulación de la ACTH se realiza mediante la corticoliberina (CRH), una hormona del hipotálamo que libera corticotropina a través del cortisol mediante un mecanismo de retroalimentación negativa. Esto significa que la deficiencia de cortisol estimula la liberación de CRH y ACTH, mientras que su exceso inhibe esta secreción. Así, la liberación de cortisol regula muchas funciones vitales importantes, como la movilización del organismo ante situaciones de estrés, el aumento de la presión arterial y las capacidades antiinflamatorias. La ACTH se secreta de forma pulsátil siguiendo un ritmo circadiano, alcanzando su concentración máxima en las horas de la mañana, cuando es más necesaria, y disminuyendo a lo largo del día. El aumento de la secreción de ACTH se observa en enfermedades como la insuficiencia suprarrenal, la enfermedad de Cushing o el síndrome de Nelson.
Insulina y péptido C
La insulina y el péptido C son secretados continuamente por el páncreas en el cuerpo humano. Durante la producción de insulina, en su proceso de biosíntesis, se produce el péptido C. Las células pancreáticas producen en la primera etapa la preproinsulina, que sufre modificaciones posteriores mediante la eliminación de aminoácidos, lo que conduce a la formación de la proinsulina compuesta por dos cadenas, A y B, unidas por el péptido C; luego, el péptido C se separa de la proinsulina, dando lugar a la forma final. Cuando aparece glucosa en el organismo, el páncreas recibe la señal para liberar gránulos con moléculas almacenadas de insulina y péptido C. El papel biológico de los aminoácidos, proteínas y péptidos es fundamental para el correcto funcionamiento y la regeneración del organismo. El péptido C se mantiene en el hígado mucho más tiempo que la insulina, ya que no se degrada allí. Su descomposición ocurre principalmente en los riñones. Tanto en la insulina como en el péptido C, concentraciones elevadas o demasiado bajas pueden conducir al desarrollo de diabetes tipo I o II, así como a la enfermedad de Cushing. En el caso del péptido C, las fluctuaciones en su concentración también pueden indicar insuficiencia renal crónica o la presencia de metástasis o recurrencia local del tumor, por lo que es muy importante mantener sus niveles dentro de los rangos normales.
Motilina
La motilina es una hormona relacionada con los músculos lisos del estómago e intestinos, controlada por fibras del nervio vago. Se sintetiza en células endocrinas. Como hormona peptídica, compuesta por 22 aminoácidos en una secuencia específica, es producida por células del intestino delgado. Producida por células endocrinas del sistema digestivo M (Mo), participa en la regulación de la motilidad del tracto gastrointestinal. La motilina es una hormona importante que interviene en la generación de la fase III del complejo motor migratorio (MMC), en la cual el estómago y el intestino delgado tienen la tarea de vaciar el estómago de restos alimentarios innecesarios y células epiteliales descamadas, estimulando los movimientos peristálticos. Además, la hormona influye en el vaciamiento de la vesícula biliar durante el período interdigestivo, cuando la concentración de motilina es máxima.
Glucagón
El glucagón es una de las hormonas involucradas en la regulación de la concentración de glucosa; este péptido es secretado por las células endocrinas del páncreas. Es un polipéptido compuesto por 29 aminoácidos, derivado de un precursor con una estructura de 180 aminoácidos. Los cambios en la concentración de glucosa permiten la secreción de glucagón. La producción de la hormona glucagón ocurre en los islotes pancreáticos, donde a partir del proglucagón se forman tanto el glucagón como el polipéptido pancreático dependiente de glicentina (GRPP). La función principal del glucagón es mantener la concentración adecuada de glucosa en el suero durante su descenso entre comidas o durante el esfuerzo físico. Sus reservas en estas situaciones se liberan desde el hígado para proporcionar al organismo la protección adecuada. Además, puede participar en la regulación durante la ingesta de alimentos, por lo que la sensación de saciedad puede aparecer antes. El glucagón potencialmente puede inhibir la liberación de grelina y también puede frenar la motilidad intestinal. Rol biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo
Hormonas proteicas
Hormona del crecimiento HGH La hormona del crecimiento HGH también se llama somatotropina. Es producida por células acidófilas que pertenecen al lóbulo anterior de la hipófisis. La hormona conduce al aumento de la proliferación celular en diversos tejidos, lo que resulta en un incremento en su número y tamaño. La HGH está compuesta por 190 aminoácidos en forma de una cadena polipeptídica simple. En el organismo se libera de forma pulsátil aproximadamente cada 3-4 horas, y sus concentraciones más altas se registran durante la noche. El proceso de secreción de la hormona está regulado por hormonas hipotalámicas con acciones opuestas. Estas hormonas incluyen la hormona liberadora de la hormona del crecimiento (GN-RH) y la hormona inhibidora de su liberación (SRIF). Durante la liberación de somatotropina, este proceso está regulado por neurohormonas: somatoliberina (GHRH), somatostatina (GHIH), grelina, glucocorticoides, ácidos grasos, glucosa, insulina y hormonas sexuales. La hormona del crecimiento regula procesos metabólicos, la modulación del crecimiento corporal, la estimulación y proliferación celular. La acción de la HGH es bastante amplia e incluye, entre otros, la estimulación del crecimiento de los huesos largos, la síntesis de ácidos nucleicos y la regulación del metabolismo de carbohidratos. La hormona del crecimiento tiene un amplio uso entre personas que practican deporte. La administración de somatotropina en deportistas influye en el fortalecimiento, construcción muscular y minimización de lesiones durante los entrenamientos, mediante el desarrollo del tejido conectivo que forma el cartílago. Al decidir tomar la hormona del crecimiento, es importante mantener otros factores como una cantidad suficiente de sueño y una dieta adecuada. Papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo
Conclusiones
Como se mencionó anteriormente, los aminoácidos, proteínas y péptidos participan en el correcto funcionamiento del organismo. En el caso de los péptidos, se puede inferir que su uso adecuado permite una terapia de salud segura, efectiva y satisfactoria. Considerando su acción, están indicados para su uso en casi todos los casos y para todas las personas. Son especialmente recomendados para deportistas con fines regenerativos y preventivos. Las deficiencias tanto de hormonas proteicas como de hormonas peptídicas pueden conducir a graves trastornos en el funcionamiento del organismo. Papel biológico de los aminoácidos, proteínas y péptidos en el correcto funcionamiento y regeneración del organismo.
Bibliografía:
- Bańkowski.E, Bioquímica. 2020; 160(1-3):33-41
- Dryweń.M, Dźwigała J, Importancia de los aminoácidos ramificados en la nutrición humana y en la prevención y curso de algunas enfermedades. Medicina General y Ciencias de la Salud; 2013; 3(1) 379-384
- Darewicz.M, Borawska J, Minkiewicz P, Péptidos biológicamente activos liberados de proteínas alimentarias. 2015; 3(100) 26-41; DOI:10.15193/zntj/2015/100/037
- Miyamoto.T, Detección y cuantificación de residuos de aminoácidos d en péptidos y proteínas mediante hidrólisis ácida. 2018; 775-782; DOI:10.1016/j.bbapap.2017.12.010
- Bottecchia.C, Modificación fotocatalítica de aminoácidos, péptidos y proteínas. 2018; 26-42; DOI:10.1002/chem.201803074
- Rutherfurd M, Análisis de aminoácidos. 2009; 11.9.1-11.9.37; DOI:10.1002/0471140864.ps1109s58
- Rob.M, Liskamp.J, Péptidos y proteínas como una fuente continua y emocionante de inspiración para peptidomiméticos. 2011; 1626-1653; DOI:10.1002/cbic.201000717
- Lewandowski K, Lewiński A, Hormonas peptídicas secretadas en el tracto gastrointestinal. 2012: 12(1) 10-14
- Klein A. Mecanismos moleculares de la regulación hormonal. Editorial de la Universidad Jagellónica. 2010; 200-233
- Marciniak. P, Szymczak.M, Hormonas peptídicas. Avances en biología celular. 2011; 43-63
- O’Neill.R, Murphy.R, Endocrinología. 2012; 30-45
- Siewko.K, Szelachowska.M, Péptido C como factor de riesgo para el desarrollo de diabetes tipo 1 en familiares de primer grado de personas con diabetes autoinmune. P2009; 60(5) 26-43
- Romański.K, Goździewska.K, Grelina y motilina: similitudes y diferencias en la regulación de la actividad motora del tracto gastrointestinal. 2008; 64(11) 5-19
- Nylec.M, Olszanecka.M, Papel del glucagón en la patogénesis de la diabetes tipo II. 2010; 1734-3321
- Hsiao.Y, Yamada.M, Los roles de las hormonas peptídicas y sus receptores durante el desarrollo de la raíz de las plantas. 2020; 12(1) 22; DOI:10.3390/genes12010022
- Imura.H, Nakai Y, Tanaka N, ACTH y péptidos relacionados. 2000; 41(5) 949-56
- Brownstein M, Hormona adrenocorticotrópica en el sistema nervioso central. 2000; 22: 93-9
- Itoh. A, Motilina y aplicación clínica. 2001; 593-608; DOI:10.1016/S0196-9781(96)00333-6 19. Chen.C, Grelina y motilina en el sistema gastrointestinal. 2012; DOI:10.2174/138161212803216915
- Drucker.D, Mecanismos de acción y aplicación terapéutica del péptido similar al glucagón-1. Metabolismo celular, 2018: 740-756; DOI:10.1016/j.cmet.2018.03.001
- Bildingmaier. M, Hormona del crecimiento. 2009; 187-200
- Lee.S, Park.H, Evaluación de la bioeficacia de una forma estabilizada de la hormona humana del crecimiento (SP-hGH). 2013; 45(10):722 -727; DOI:10.1055/s-0033-1345126
- Maciejewska.Z, Korek.E, Papel de la hormona del crecimiento, factor de crecimiento similar a la insulina tipo 1 y grelina. 2016; 216-220





¡BPC-157 Producto del año 2020! ¡Innovación en primer lugar!
Acción neuroprotectora y antidepresiva de BPC-157. Influencia de BPC-157 en el funcionamiento cerebral.